吉美瑞生气道基底层干细胞产品获FDA孤儿药认定(ODD)
发布时间:25/02/07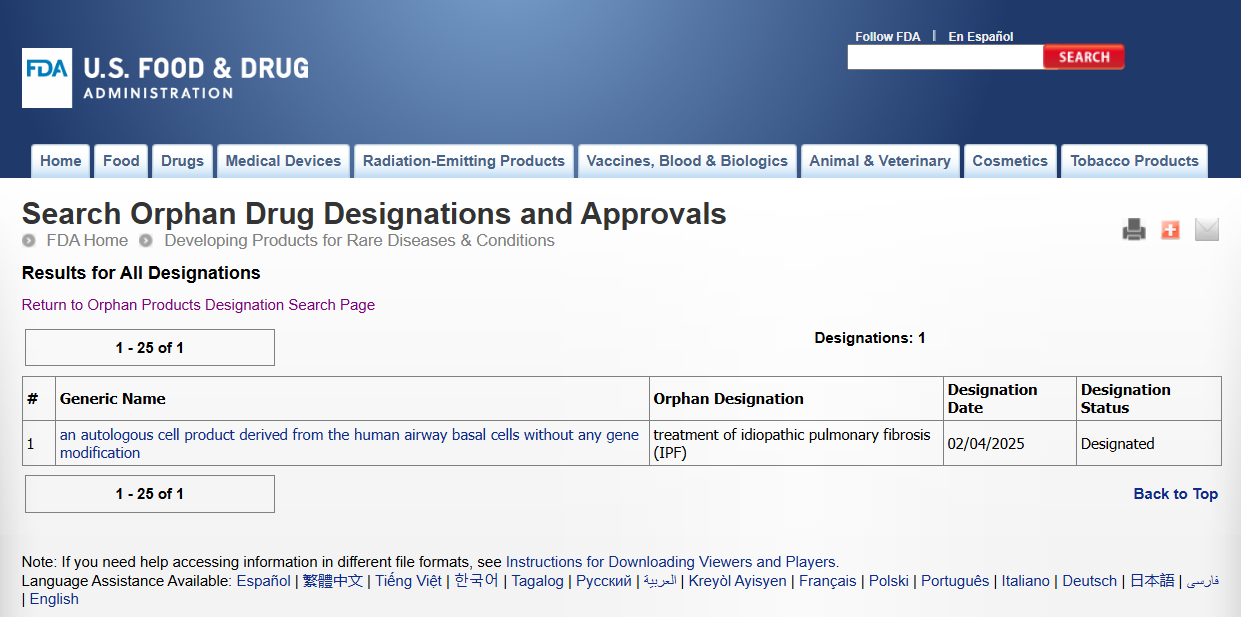
吉美瑞生董事长左为教授对此表示:“我们非常高兴Pulmovinci获得FDA授予的治疗IPF的孤儿药资格认定。IPF是一种预后极差的疾病,患者通常在确诊后2至3年内面临生命危险。这一监管里程碑标志着Pulmovinci作为IPF潜在新疗法的开发迈出了重要一步,后续我们将推进其在美国的临床试验,将肺脏再生修复技术早日惠及全球患者。”

吉美瑞生董事长左为教授对此表示:“我们非常高兴Pulmovinci获得FDA授予的治疗IPF的孤儿药资格认定。IPF是一种预后极差的疾病,患者通常在确诊后2至3年内面临生命危险。这一监管里程碑标志着Pulmovinci作为IPF潜在新疗法的开发迈出了重要一步,后续我们将推进其在美国的临床试验,将肺脏再生修复技术早日惠及全球患者。”